Aging Cell | 郭莲仙与邵义明教授团队揭示了肠道微生物代谢物如何驱动系统性衰老和多器官氧化还原变化
最近,我校公共卫生学院郭莲仙教授与东莞附属第一医院邵义明教授团队在中国科学院权威期刊Aging Cell上发表了题为A Multi-Organ Atlas Links Gut Microbial Metabolites to Systemic Redox Changes in Aging Mice的研究论文。这项突破性研究提供了首个全面的多器官图谱,将肠道衍生代谢重编程与系统氧化还原变化联系起来,提供了潜在的干预衰老的靶点。

衰老是一个普遍的过程,但肠道微生物代谢物如何驱动特定器官功能衰退的具体机制仍不甚明了。虽然与年龄相关的分子特征如线粒体功能障碍、氧化应激和慢性炎症已有充分文献记载,但这些肠道来源的压力源协调传播到全身循环和远端组织的过程却缺乏一个完全整合的框架。
为应对这一科学挑战,研究团队利用拟靶向代谢组学(Pseudotargeted Metabolomics)技术,开发了一套全面的多组学图谱,研究年轻和衰老的小鼠的肠道、血清、肝脏、肺部和大脑皮质代谢谱。研究揭示了一个保守的衰老特征,该特征由微生物群相关保护性循环代谢产物(如溶磷脂酰胆碱(LPCs)的耗尽,以及促氧化微生物catabolite(特别是三甲胺N-氧化物TMAO)和吲哚-3-乙酸(IAA)的系统性积累所定义。团队证明,这种微生物-代谢漂移从根本上破坏了全身脂质运输和氧化还原平衡。关键是,这种破坏导致了器官层面的明显脆弱性:肝脏会出现脂质堆积和铁消亡的易感性,肺部表现出免疫氧化还原激活,皮质则出现严重的神经化学失调。
为确定这些发现的功能和因果相关性,研究团队对40项独立研究进行了综合荟萃分析,涵盖自然衰老模型、粪便微生物移植(FMT)和益生菌干预,证实重塑肠道微生物群能通过上调ZO-1和MUC2等必需蛋白,有效恢复肠道屏障完整性。此外,这些靶向干预措施被证明能抑制组织炎症因子(IL-6、IL-1β、TNF-α),并通过降低MDA水平和恢复SOD和GSH抗氧化能力,减轻远端氧化应激。这些发现凸显了肠道微生物重编程作为可调节的上游驱动因子,能够逆转系统性炎症和氧化应激导致的衰劳。
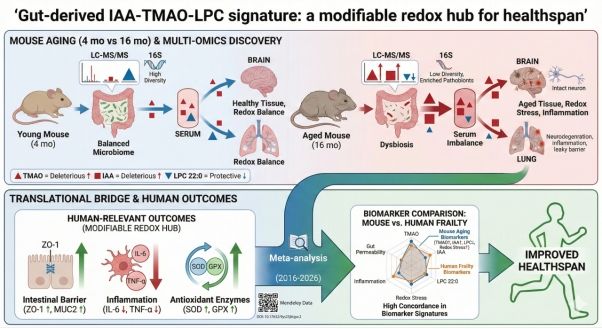
(研究机制示意图)
该论文的第一作者分别是我校公共卫生学院博士后Sanaullah Sajid 和2021级卫生毒理学研究生黄杰良,该工作得到了国家自然科学基金(82273757、82574226)、广东省自然科学基金(2023B1515020106)以及广东医科大学学科建设项目(4SG25295G,4SG25239G)的支持。
论文链接:https://onlinelibrary.wiley.com/doi/full/10.1111/acel.70433。




