广东医科大学陈家隆团队、南方医科大学邹飞教授团队合作揭示帕金森病新机制:Parkin经分子伴侣介导自噬降解NLRP3抑制泛凋亡,保护多巴胺能神经元
帕金森病(PD)的核心病理特征是黑质致密部多巴胺能(DA)神经元的选择性死亡。近日,广东医科大学陈家隆团队、南方医科大学邹飞教授团队、东莞市人民医院夏婷婷合作,在神经炎症领域权威期刊《Journal of Neuroinflammation》发表题为Parkin regulates NLRP3 degradation through chaperone-mediated autophagy to suppress PANoptosis and protect dopaminergic neurons in Parkinson’s disease的最新研究,系统揭示了Parkin通过介导NLRP3 K353位点泛素化,促进CMA依赖性NLRP3降解,进而抑制DA神经元泛凋亡(PANoptosis)的全新分子机制。
泛凋亡是整合焦亡、凋亡、坏死性凋亡的炎症性程序性细胞死亡方式,是介导PD中DA神经元退变死亡的关键通路。NLRP3炎症小体是PANoptosis的关键上游激活因子。研究团队利用鱼藤酮诱导的SN4741细胞和小鼠PD模型发现:Parkin可直接与NLRP3相互作用,并特异性泛素化其K353位点;该泛素化修饰促进NLRP3通过分子伴侣介导的自噬(CMA)途径降解。由此,Parkin有效抑制NLRP3驱动的PANoptosis,从而保护多巴胺能神经元。
进一步实验表明,将NLRP3的K353位点突变为精氨酸(K353R)后,NLRP3无法被Parkin有效泛素化,亦不能被CMA有效降解,反而加剧PANoptosis和神经元损伤。此外,使用NLRP3抑制剂MCC950或CMA激活剂CA77.1,均能减轻PD模型中的神经元损伤和运动功能障碍。
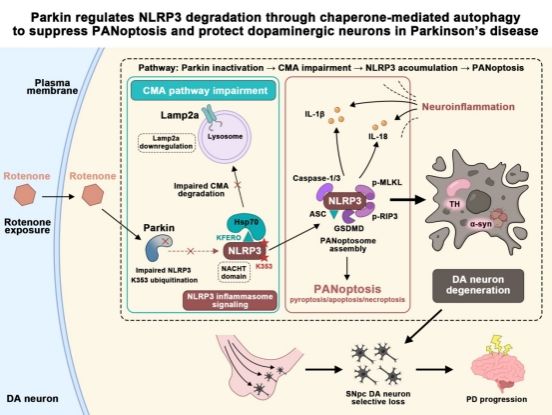
该研究首次阐明了“Parkin–NLRP3–CMA–PANoptosis”信号轴在帕金森病中的关键作用,为靶向CMA激活剂或NLRP3抑制剂的疾病修饰治疗策略提供了新思路。
本论文共同第一作者为广东医科大学郑冬燕、张贺、谢艾伦。广东医科大学陈家隆副教授、南方医科大学邹飞教授及东莞市人民医院夏婷婷医生是这一研究成果的共同通讯作者。研究工作得到了国家自然科学重点基金、广东省自然科学基金、广东医科大学临床+基础重点项目等的资助。
原文链接:https://doi.org/10.1186/s12974-026-03814-2




