崔理立教授团队发表系列研究揭示阿尔兹海默病易感基因致病新机制
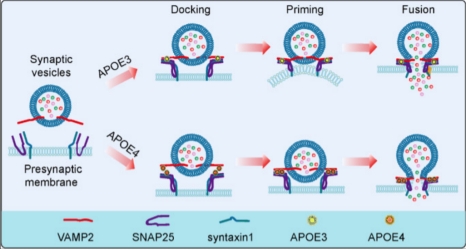
广东医科大学海洋与热带医学学院崔理立教授团队在国际学术期刊《Cellular and Molecular Life Sciences》(中科院TOP期刊)发表题为“APOE4 triggers dysregulated synaptic vesicle release by disrupting SNARE complex assembly”的研究论文,首次揭示了载脂蛋白E4(APOE4)通过破坏SNARE复合物的液-液相分离,进而阻碍其组装,抑制突触囊泡释放,增加神经退行性疾病风险的分子机制。该成果阐明了APOE基因多态性的致病机理,为相关靶向治疗提供了理论依据。
 |
此外,该团队还在《Cell Communication and Signaling》(中科院TOP期刊)上发表题为“De-2-hydroxyisobutyrylation of clusterin modulates neuropathology and memory deficits in an Alzheimer's disease mouse model”的研究论文。该研究发现,降低阿尔茨海默病(AD)模型小鼠脑内簇集蛋白(CLU)第436位赖氨酸(K436)的2-羟基异丁酰化(Khib)修饰水平,能够减少淀粉样斑块沉积、减轻神经炎症、改善记忆缺陷并恢复脑细胞功能,提示靶向CLU蛋白的Khib修饰有望成为AD治疗的新策略。
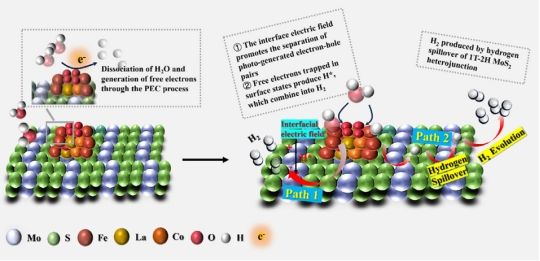
近日,广东医科大学我校海洋与热带医学学院李妍锌/崔理立团队与中国海洋大学曹立新/李海艳教授在Advanced Functional Materials期刊发表题为“1T/2H MoS2 Functional Layer Boosts HER Kinetics of LaFeO3 Photocathode in Neutral Media through Hydrogen Spillover and Surface State Regulation”的研究论文,本研究开发了一种高效电子空间分离及传输功能异质结催化剂Co-LFO/1T-2H MoS₂,用于高效光电化学水分解制氢。
LaFeO₃(LFO)是一种典型的p型半导体,因其合适的能带结构和组成灵活性而成为PEC水分解中极具吸引力的阴极材料。然而,严重的载流子复合和缓慢的电荷/质子传输动力学尤其是在中性条件下严重限制了其应用。
为解决这些问题,本研究首先通过钴掺杂(Co-LFO)来调控LFO的电子结构并提升其电荷传输性能。随后,在Co掺杂LFO的基础上,创新性地引入了2H-1T MoS₂同质结功能层(Co-LFO/1T-2H MoS₂),以扩展催化剂的光吸收范围和提升光生载流子分离效率。此外,实验与密度泛函理论(DFT)计算结果显示,2H-1T MoS₂通过氢溢流效应和表面态调制作用,加速了Co-LFO光阴极的载流子分离/传输动力学。
本研究提供了有效的电子传输提升与表面电子调控策略有望应用于催化医学领域,为生物医学功能材料(如抗菌界面、药物载体、生物传感器)的设计提供了全新的思路,为未来在抗感染治疗、海洋药物合成等方向的发展提供了新的潜在应用方法。
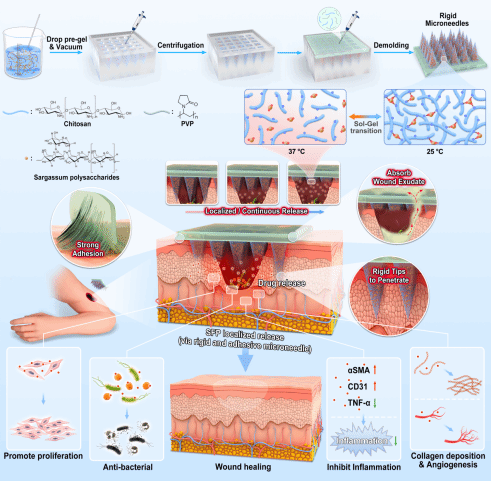
近日广东医科大学海洋与热带医学学院吴科锋研究员课题组在国际知名期刊《Carbohydrate Polymers》发表了题为“An adhesive chitosan microneedle patch incorporating a Sargassum-derivedpolysaccharide for skin repair”的研究论文,文章报道了一种新型的兼具强大组织黏附性与持续药物释放功能的凝胶微针贴片。文章第一作者为欧阳茜茜博士,现为广东医科大学海洋与热带医学学院讲师,从事纳米材料与水凝胶材料在生物医学领域的应用研究,以及广东医科大学硕士研究生屈洪娇。文章通讯作者为香港中文大学谢宪博士与广东医科大学海洋与热带医学学院吴科锋研究员。
微针贴片在伤口修复领域应用前景广阔。然而,其临床实用性却因附着性差及界面稳定性不足而受到限制,这往往会导致伤口二次开裂和药物递送效率低下。近期,广东医科大学吴科锋研究员课题组报道了一种源自海洋的粘附性微针贴片,巧妙地将牢固的组织粘附性与持续的药物释放结合起来,以实现有效的皮肤再生。该水凝胶贴片能够吸收伤口渗出液,并在组织表面形成机械稳定的粘附,从而实现长效固定并保护创面;同时,凝胶微针具有坚硬、尖锐的锥形尖端,不仅能有效穿透皮肤,还能通过共形接触和氢键作用确保牢固的界面粘附。这种紧密的微针-组织整合,实现了抗菌多糖在伤口界面的局部、持续释放,保障了治疗效果的持久性。该微针贴片能够加速伤口闭合、促进胶原蛋白沉积、刺激血管新生并减轻炎症反应。该海藻来源的微针贴片作为一个能稳定伤口界面、增强治疗递送的多功能平台,在多种生物医学应用中展现出巨大潜力。